Kinetiikka tutkii kemiallisen reaktion kulkua, reaktiomekanismeja ja reaktionopeuksia. Kemialliset reaktiot ovat tarkalleen ottaen elektronien siirtoreaktioita, joissa lähtöaineiden kemialliset sidokset katkeavat ja syntyy uusia sidoksia.
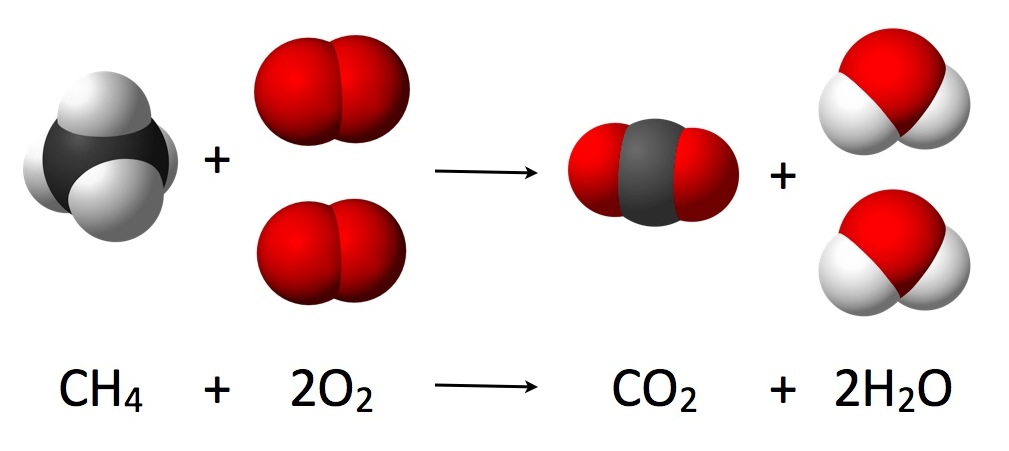
Lähtöaineiden vahvojen sidosten katkeaminen vaatii aina energiaa. Tämän energian suuruutta kuvastaa reaktion aktivoitumisenergia, tai aktivaatiokynnys. Jotta reaktio saadaan aikaan, kynnys on ylitettävä tuomalla systeemiin lisäenergiaa esimerkiksi tarpeeksi suuren lämpötilan avulla, jotta reagoivat aineet törmäävät toisiinsa riittävän suurella energialla.
Aktivoitu kompleksi tarkoittaa välituotetta, joka syntyy yhdisteiden törmättyä ja sidosten rikkouduttua. Tämän jälkeen atomit tai ionit alkavat sitoutua uudella tavalla.
Kun uusia sidoksia syntyy, vapautuu energiaa.
Jos vapautunut energia on suurempi, kuin vaadittu energia sidosten katkeamiselle, reaktion sanotaan olevan eksoterminen reaktio. Yleensä energiaa vapautuu aineiden ympäristöön lämpönä, mutta usein vapautunut energia voidaan havaita myös valona, äänenä ja syntyneiden kaasujen liike-energiana.
Muussa tapauksessa vapautunut energia jää pienemmäksi kuin aktivoitumisenergia, jolloin reaktio sitoo energiaa ympäristöstään mm. lämpönä tai sähkömagneettisena säteilynä (UV-säteily, näkyvä valo tai infrapunasäteily).
Reaktiossa vapautunutta tai sitoutunutta energiaa kutsutaan nimellä reaktiolämpö, eli entalpiamuutos.
Eksotermiselle reaktiolle
Endotermiselle reaktiolle
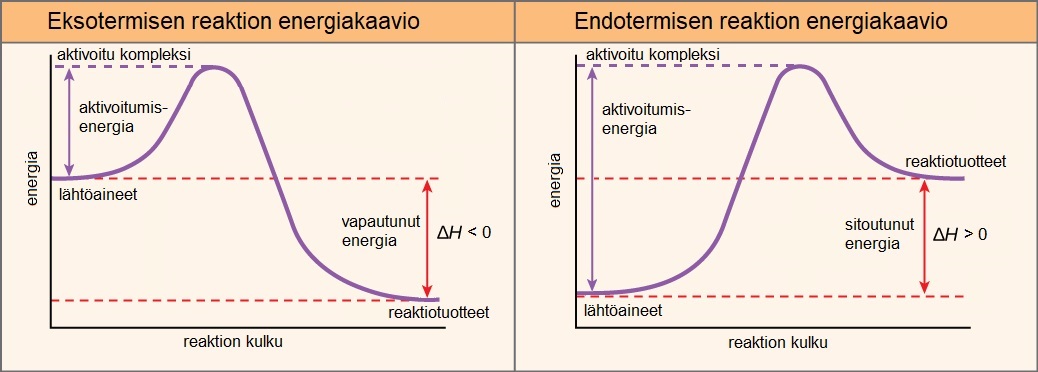
Figure 2:Ekso- ja endotermisen reaktion energiakaaviot. Kuvan alkuperäinen tekijä: CNX OpenStax, lähde: Wikipedia
Entalpia¶
Aineen sisältämää kemiallista energiaa sanotaan entalpiaksi. Entalpiaa merkitään tunnuksella H ja yksikkönä on joule, J. Entalpian suuruutta eli aineen energiasisältöä ei voida mitata mutta sen muutos on mahdollista määrittää joko kokeellisesti tai tunnettujen osareaktioiden avulla. Kokeellisesti reaktiossa vapautuvan tai sitoutuvan lämpöenergian määrä voidaan mitata kalorimetrisin mittauksin mittaamalla lämpötilamuutoksia eristetyssä, suljetussa systeemissä. Laskennallinen entalpianmuutos (ΔH) eli reaktiolämpö määritellään reaktiotuotteiden ja lähtöaineiden entalpioiden kautta. ∆H ilmoitetaan kertoimien ilmoittamia moolimääriä kohti, joka on vakiopaineessa sama kuin reaktiotuotteiden ja lähtöaineiden välinen entalpiaero:
Muodostumislämpö¶
Aineen muodostumislämmöllä tarkoitetaan sitä entalpiamuutosta, joka syntyy, kun yksi mooli ainetta syntyy alkuaineistaan olosuhteissa T = 298.15 K ja p = 101.325 kPa. Alkuaineen pysyvimmän muodon entalpia on annetuissa olosuhteissa 0 kJ/mol.
Hessin laki¶
Entalpiamuutos eli reaktiolämpö on riippumaton siitä, tapahtuuko reaktio suoraan vai välivaiheiden (osareaktioiden) kautta. Hessin lain mukaan reaktion entalpia voidaan laskea osareaktioiden avulla. Lain avulla voidaan täten määrittää minkä tahansa reaktion reaktiolämpö, jos kokonaisreaktion osareaktioiden reaktiolämmöt tunnetaan.
\begin{equation*} \begin{array}{ c c c } \mathrm{Lähtöaineet} & \xrightarrow[]{\Delta H} & \mathrm{Reaktiotuotteet} \\ \uparrow & & \uparrow \\ \Delta H_{lähtöaineet} & & \Delta H_{tuotteet} \\ & \mathrm{Aineet} & \\ \end{array} \end{equation*}

Figure 4:Hessin laki, jos koodimuotoinen kuva ei yllä toimi.
Olomuodon muutokset ja entalpia¶
Reaktionopeuteen vaikuttavat tekijät¶
Kemiallisen reaktion nopeuteen vaikuttavat
Systeemin lämpötila (törmäysenergian suuruus)
Aineiden sekoittuminen (törmäysten todennäköisyys)
Aineiden hienojakoisuus (kosketus- eli vuorovaikutuspinta-ala)
Paine (törmäyksiä aikayksikössä)
Katalyytti / Katalysaattori (muuttaa reaktiomekanismia ja alentaa siten aktivoitumisenergiaa, mutta ei itse kulu reaktiossa. Luonnon katalyytti = entsyymi)
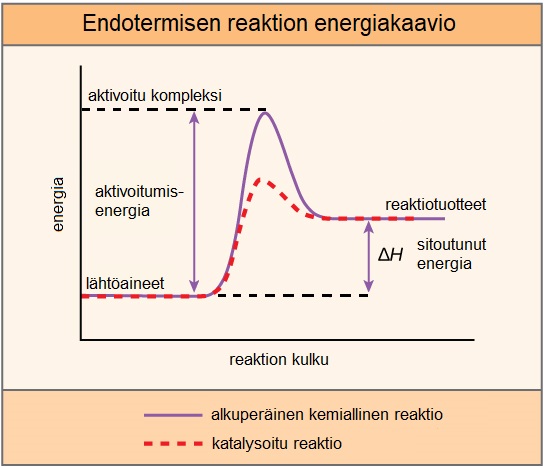
Figure 6:Katalyytin vaikutus endotermisen reaktion aktivoitumisenergiaan. Kuvan alkuperäinen tekijä: CNX OpenStax, lähde: Wikipedia